พันธะโลหะสมบัติ
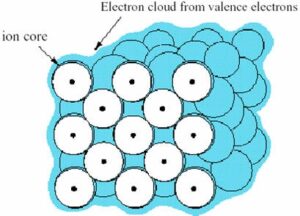
พันธะโลหะ (Metallic bonding) เป็นพันธะภายในโลหะซึ่งเกี่ยวข้องกับ การเคลื่อนย้าย อิเล็กตรอน อิสระระหว่าง
แลตทิซของอะตอมโลหะดังนั้นพันธะโลหะจึงอาจเปรียบได้กับเกลือที่หลอมเหลวอะตอมของโลหะมีอิเล็กตรอนพิเศษ
เฉพาะในวงโคจรชั้นนอกของมันเทียบกับคาบ(period)หรือระดับพลังงานของพวกมัน อิเล็กตรอนที่เคลื่อนย้ายเหล่านี้
เปรียบได้กับทะเลอิเล็กตรอน(Sea of Electrons) ล้อมรอบแลตทิชขนาดใหญ่ของไอออนบวกพันธะโลหะเทียบได้
กับพันธะโควาเลนต์ที่เป็น นอน-โพลาร์ ที่จะไม่มีในธาตุโลหะบริสุทธ์ หรือมีน้อยมากในโลหะผสม ความแตกต่าง อิเล็ก
โตรเนกาทิวิตีระหว่างอะตอม ซึ่งมีส่วนในปฏิกิริยาพันธะ และอิเล็กตรอนที่เกี่ยวข้องในปฏิกิริยาจะเคลื่อนย้ายข้าม
ระหว่างโครงสร้างผลึกของโลหะ พันธะโลหะเขียนสูตรทางเคมีไม่ได้ เพราะไม่ทราบจำนวนอะตอมที่แท้จริง อาจจะมีเป็น
ล้านๆ อะตอมก็ได้ พันธะโลหะจะมีความสำคัญต่อคุณสมบัติทางฟิสิกส์หลายอย่างของโลหะเช่น
– ความแข็งแรง
– ตีแผ่เป็นแผ่นได้(malleability)
– ดึงเป็นเส้นได้ (ductility)
– นำความร้อนไดดี
– นำไฟฟ้าได้ดีและนำได้ทุกทิศทาง
– เนื้อเป็นเงา (luster)
การเกิดพันธะเคมี
1. โลหะมีค่าพลังงานไอออไนเซชั่นต่ำมาก แสดงว่าอิเล็กตรอนของโลหะจะหลุดออกไปได้ง่าย เมื่อวาเลนซ์
อิเล็กตรอนหลุดออกไป ก็จะเหลืออนุภาคบวกดังนี้
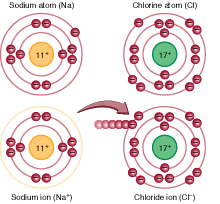
โลหะทุกอะตอมเป็นตัวให้อิเล็กตรอนทั้งสิ้นดังนั้นจะไม่มีอะตอมใดเลยที่ได้รับอิเล็กตรอน
2. โลหะมีเวเลนซ์อิเล็กตรอนน้อย ดังนั้นอิเล็กตรอนที่หลุดออกไป จะมีเพียง 1,2,3 ตัวเท่านั้น
3. โลหะมีค่าโคออร์ดิเนชั่นนัมเบอร์สูง ซึ่งเท่ากับ 8 หรือ12 หมายความว่า อะตอมหนึ่งจะมีอะตอมอื่นรอบล้อม 8 ถึง
12 อะตอมดังนั้นการนำอิเล็กตรอนมาใช้ร่วมกันเป็นอิเล็กตรอนคู่ในลักษณะของพันธะโคเวเลนต์จึงเป็นไปไม่ได้
ดังนั้นการเกิดพันธะโลหะควรเป็นไปในลักษณะที่ว่าเวเลนซ์อิเล็กตรอนของอะตอมโลหะ ที่หลุดออกไปจะไม่เป็น
ของอะตอมใดอะตอมหนึ่งโดยเฉพาะแต่จะเป็นของอะตอมทั้ง หมด โดยที่อิเล็กตรอนจะเคลื่อนที่ไปยังอะตอมนี้บ้าง
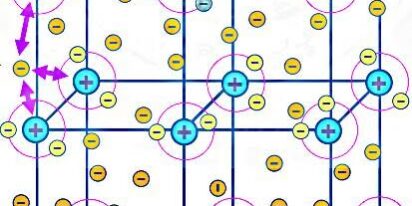
อะตอมโน้นบ้าง ในผลึกของโลหะจึงเป็นการเอาอนุภาคบวกมาเรียงกัน ไว้อย่างมีระเบียบ และมีเวเลนซ์อิเล็กตรอน
เคลื่อนที่ไปมาได้ทั่วอนุภาคบวกทั้งหมด หรืออาจกล่าวได้ว่า อนุภาคบวกเหล่านั้นจมอยู่ในทะเลอิเล็กตรอน แรงดึงดูด
ระหว่างอนุภาคบวกกับอิเล็กตรอนเรียกว่า “พันธะโลหะ” ซึ่งมีแรงยึดเหนี่ยวระหว่างพันธะแข็งแรงมาก