การจัดเรียงอิเล็กตรอน

จากการเรียงอิเล็กตรอนของธาตุในระดับพลังงานหลักทำให้ทราบว่า
1. จำนวนระดับพลังงานหลักของอิเล็กตรอน ทำให้ทราบว่าธาตุนั้นอยู่คาบใด ถ้าธาตุมีจำนวนระดับพลังงานของอิเล็กตรอนเท่ากัน แสดงว่าธาตุนั้นอยู่ในคาบเดียวกัน เช่น
Mg มีเลขอะตอม 12 มีการจัดอิเล็กตรอนในระดับพลังงานดังนี้ 2, 8, 2 Mg มี 3 ระดับพลังงาน
S มีเลขอะตอม 16 มีการจัดอิเล็กตรอนในระดับพลังงานดังนี้ 2, 8, 6 S มี 3 ระดับพลังงาน
แสดงว่า Mg และ S อยู่ในคาบเดียวกัน
2 จำนวนเวเลนซ์อิเล็กตรอน หรืออิเล็กตรอนที่อยู่ในระดับพลังงานนอกสุด ทำให้ทราบหมู่ของธาตุ ถ้าธาตุมีจำนวนเวเลนซ์อิเล็กตรอนเท่ากัน แสดงว่าธาตุนั้นอยู่ในหมู่เดียวกัน เช่น
Na มีเลขอะตอม 11 มีการจัดอิเล็กตรอนในระดับพลังงานดังนี้ 2, 8, 1 Na มีเวเลนซ์อิเล็กตรอนเท่ากับ 1
K มีเลขอะตอม 19 มีการจัดอิเล็กตรอนในระดับพลังงานดังนี้ 2, 8,8, 1 K มี เวเลนซ์อิเล็กตรอนเท่ากับ
แสดงว่า ธาตุ Na และ K อยู่ในหมู่เดียวกัน
การจัดเรียงอิเล็กตรอนในระดับพลังงานย่อย
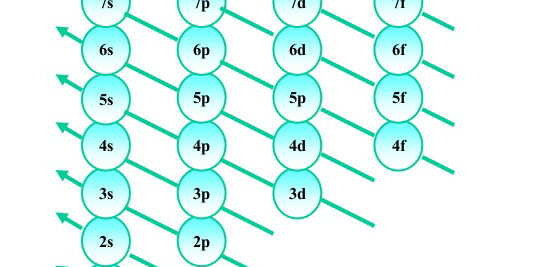
การจัดอิเล็กตรอนในระดับพลังงานหลัก ทำให้แต่ละระดับพลังงานมีจำนวนอิเล็กตรอนมากจึงเกิดปัญหาว่าอิเล็กตรอนเหล่านั้นอยู่ในระดับพลังงานเดียวกันได้อย่างไร ทำไมจึงไม่ผลักกัน เพื่อแก้ปัญหาดังกล่าว นักวิทยาศาสตร์จึงได้ศึกษาเกี่ยวกับระดับพลังงานย่อยเพื่อกระจายอิเล็กตรอนในแต่ละระดับพลังงานหลัก เข้าสู่ระดับพลังงานย่อย โดยอาศัยรูปแบบโคจรของอิเล็กตรอนรอบ ๆ นิวเคลียสเป็นเกณฑ์ในการแบ่งอิเล็กตรอนเป็นกลุ่มย่อย ๆ และเรียกรูปแบบวงโคจรนี้ว่าออร์บิทัล (Orbital) โดย 1 ออร์บิทัลจะมีอิเล็กตรอนได้ไม่เกิน 2 อิเล็กตรอน ระดับพลังงานย่อยมี 4 ระดับ คือ s, p, d, f โดยระดับพลังงานย่อยมี
s มี 1 ออร์บิทัล บรรจุอิเล็กตรอนได้สูงสุด 2 อิเล็กตรอน
p มี 3 ออร์บิทัล บรรจุอิเล็กตรอนได้สูงสุด 6 อิเล็กตรอน
d มี 5 ออร์บิทัล บรรจุอิเล็กตรอนได้สูงสุด 10 อิเล็กตรอน
f มี 7 ออร์บิทัล บรรจุอิเล็กตรอนได้สูงสุด 14 อิเล็กตรอน
|
|
|
| ข้อสังเกตที่ได้จากการใช้จัดเรียงอิเล็กตรอนในอะตอม
1. เลขอะตอมคู่จะอยู่ในหมู่คู่ เลขอะตอมคี่จะเป็นธาตุในหมู่คี่ เช่น ธาตุ 14Si จะเป็นธาตุในหมู่ 4 ธาตุ 11Na จะเป็นธาตุในหมู่ 1 2. ธาตุหมู่ IA และ IIA ตั้งแต่คาบ 3 ขึ้นไป จะมีจำนวนอิเล็กตรอนในระดับพลังงานถัดจากวงนอกสุดเข้ามา 1 ชั้นเป็น 8 เสมอ เช่น 11Na จะจัดเรียงอิเล็กตรอนเป็น 2, 8, 1 12Mg จะจัดเรียงอิเล็กตรอนเป็น 2, 8, 2 19K จะจัดเรียงอิเล็กตรอนเป็น 2, 8, 8, 1 20Ca จะจัดเรียงอิเล็กตรอนเป็น 2, 8, 8, 2 3. ธาตุหมู่ IIIA ถึง VIIIA ตั้งแต่หมู่ที่ IIIA คาบ 4 เป็นต้นไป จะมีจำนวนอิเล็กตรอนในระดับพลังงานถัดจากวงนอกสุดเข้ามา 1 ชั้นเป็น 18 เสมอ เช่น 31Ga 2, 8, 18, 3 (หมู่ 3 คาบ 4) 33As 2, 8, 18, 5 (หมู่ 5 คาบ 4) 4. ถ้าธาตุนั้นมีการจัดเรียงอิเล็กตรอนไม่เป็นไปตามข้อ 2 และ 3 คือมีจำนวนอิเล็กตรอนในระดับพลังงานถัดจากวงนอกสุดเข้ามา 1 ชั้น มีค่าตั้งแต่ 9 – 18 แต่วงนอกสุดมีเวเลนซ์อิเล็กตรอนเป็น 1หรือ 2 นักเรียนก็ทำนายได้ทันทีว่าเป็นธาตุแทรนซิชัน เช่น 29Cu 2, 8, 18, 1 ไม่ใช่เป็นธาตุหมู่ 1 แต่เป็นธาตุแทรนซิชันจัดเรียงอิเล็กตรอนเป็น 2, 8,18, 1 23V 2, 8, 8, 5 ไม่ใช่เป็นธาตุหมู่ 1 แต่เป็นธาตุแทรนซิชันจัดเรียงอิเล็กตรอนเป็น 2, 8,11, 2 หมายเหตุ ธาตุแทรนซิชันที่มีเลขอะตอมตั้งแต่ 21 – 30 จะมีเวเลนซ์อิเล็กตรอนเป็น 2 ยกเว้น Cu กับCr จะมีเวเลนซ์อิเล็กตรอนเป็น 1 |