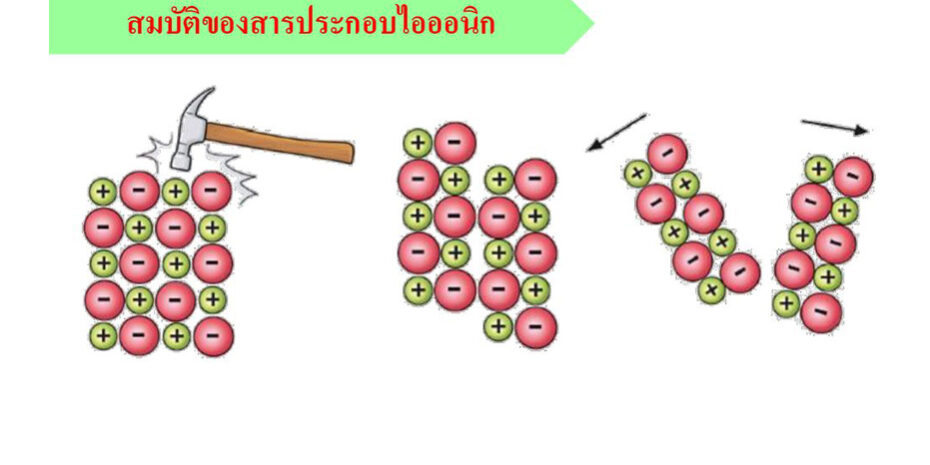
จากลักษณะการสร้างพันธะไอออนิก ซึ่งมีแรงยึดเหนี่ยวต่อเนื่องกันเป็นผลึก และลักษณะอะตอมของธาตุที่มีประจุเป็นไอออนบวกและไอออนลบรวมกันอยู่ ส่งผลให้สารประกอบไอออนิกมีสมบัติต่าง ๆ ดังนี้
1. สารประกอบไอออนิกจะมีจุดหลอมเหวและจุดเดือดที่สูง เนื่องจากพันธะไอออนิกเกิดจากแรงยึดเหนี่ยวของประจุไฟฟ้าซึ่งมีความแข็งแรงสูง ยากต่อการทำให้แยกออกจากกัน อีกทั้งยังมีลักษณะการยึดเหนี่ยวที่ต่อเนื่องกันผลึก การที่จะทำให้สารประกอบไอออนิกเปลี่ยนสถานะจึงต้องอาศัยพลังงานจำนวนมากในการทำลายแรงยึดเหนี่ยว ดังนั้นสารประกอบไอออนิกจึงมีจุดหลอมเหลวและจุดเดือดที่สูงกว่าสารประกอบโคเวเลนต์
2. สมบัติที่สำคัญอีกประการของสารประกอบไอออนิก คือ เมื่อเป็นของแข็งจะไม่นำไฟฟ้า แต่จะนำไฟฟ้าได้ดีเมื่ออยู่ในสถานะของเหลวหรือเมื่ออยุ่ในสภาพของสารละลาย เนื่องจากในสถานะของแข็งไอออนต่าง ๆ ซึ่งมีประจุไฟฟ้าจะถูกยึดเหนี่ยวกันอย่างเหนียวแน่น แต่เมื่อนำไปหลอมเหลวหรือนำไปละลายน้ำ โครงผลึกจะหลุดออกเสียสภาพไปทำให้ไอออนสามารถเคลื่อนที่ไปมาได้ สารประกอบไอออนิกจึงสามารถนำไฟฟ้าได้
สรุป สมบัติของสารประกอบไอออนิก
1. มีขั้ว เพราะสารประกอบไอออนิกไม่ได้เกิดขึ้นเป็นโมเลกุลเดี่ยว แต่จะเป็นของแข็งซึ่งประกอบด้วยไอออนจำนวนมาก ซึ่งยึดเหนี่ยวกันด้วยแรงยึดเหนี่ยวทางไฟฟ้า
2. ไม่นำไฟฟ้าเมื่ออยู่ในสภาพของแข็ง แต่จะนำไฟฟ้าได้เมื่อใส่สารประกอบไอออนิกลงในน้ำ ไอออนจะแยกออกจากกัน ทำให้สารละลายนำไฟฟ้าในทำนองเดียวกันสารประกอบที่หลอมเหลวจะนำไฟฟ้าได้ด้วยเนื่องจากเมื่อหลอมเหลวไอออนจะเป็นอิสระจากกัน เกิดการไหลเวียนอิเล็กตรอนทำให้อิเล็กตรอนเคลื่อนที่จึงเกิดการนำไฟฟ้า
3 . มีจุหลอมเหลวและจุดเดือดสูง ความร้อนในการทำลายแรงดึงดูดระหว่างไอออนให้กลายเป็นของเหลวต้องใช้พลังงานสูง
ตารางแสดงจุดหลอมเหลว และจุดเดือดของสารประกอบไอออนิกบางชนิด
สารประกอบไอออนิก สูตรโมเลกุล จุดหลอมเหลว (๐C) จุดเดือด (๐C)
โซเดียมไฮดรอกไซด์ NaOH 318 1390
โพแทสเซียมไนเดรต KNO3 334 400
แคลเซียมคลอไรด์ CaCl2 772 มากกว่า 1600
โซเดียมคลอไรด์ NaCl 801 1465
อะลูมิเนียมออกไซด์ Al2O3 2054 2980
แมกนีเซียมออกไซด์ MgO 2800 3600
4 . สารประกอบไอออนิกทำให้เกิดปฏิกิริยาไอออนิก คือ ปฏิกิริยาระหว่างไอออนกับไอออน ทั้งนี้เพราะสารไอออนิกจะเป็นไอออนอิสระในสารละลาย ปฏิกิริยาจึงเกิดทันที
5 . สมบัติไม่แสดงทิศทางของพันธะไอออนิก สารประกอบไอออนิกเกิดจากไอออนที่มีประจุตรงกันข้ามรอบ ๆ ไอออนแต่ละไอออนจะมีสนามไฟฟ้าซึ่งไม่มีทิศทาง จึงทำให้เกิดสมบัติไม่แสดงทิศทางของพันธะไอออนิก
6. เป็นผลึกแข็ง แต่เปราะและแตกง่าย