สมบัติของธาตุตามตารางธาตุ
ธาตุในแนวตั้ง แบ่งเป็น 2 กลุ่มใหญ่ ๆ คือกลุ่ม A และ B ซึ่งกลุ่ม A มี 8 หมู่ คือ IA ถึง VIIIA มีรายละเอียดของแต่ละหมู่ ดังนี้
หมู่ IA มีชื่อว่า โลหะอัลคาไล ( alkalai metals ) มีสมบัติเป็นโลหะที่มีความว่องไวในปฏิกิริยามาก มีอิเล็กตรอนวงนอกสุด 1 ตัว
– หมู่ IIA มีชื่อว่า โลหะอัลคาไลน์เอิร์ท ( alkalaine earth metals ) มีสมบัติเป็นโลหะ มีอิเล็กตรอนวงนอกสุด 2 ตัว ธาตุที่ว่องไวในปฏิกิริยาที่สุดในหมู่นี้คือ เรเดียม ( Ra )
– หมู่ IIIA ประกอบด้วยโลหะและอโลหะ มีอิเล็กตรอนวงนอกสุด 3 ตัว
– หมู่ IVA มีอิเล็กตรอนวงนอกสุด 4 ตัว
– หมู่ VA มีอิเล็กตรอนวงนอกสุด 5 ตัว
– หมู่ VIA ตอนต้นหมู่จะมีธาตุที่มีสมบัติเป็นอโลหะ แล้วค่อย ๆ เป็นโลหะ
– หมู่ VIIA มีชื่อว่า แฮโลเจน ( Halogens ) ธาตุหมู่นี้เป็นอโลหะที่ว่องไวต่อปฏิกิริยามาก
กลุ่ม B มี 8 หมู่ คือ IB ถึง VIIIB เรียกว่า ธาตุทรานซิชัน ( Transition elements ) ได้แก่
– Lanthanide series ประกอบด้วยธาตุที่มีเลขอะตอม 57 – 71 เป็นธาตุที่หายากมาก
– Actinide series ประกอบด้วยธาตุที่มีเลขอะตอม 89 – 103 ธาตุหมู่นี้มีคุณสมบัติเป็นสารกัมมันตรังสี
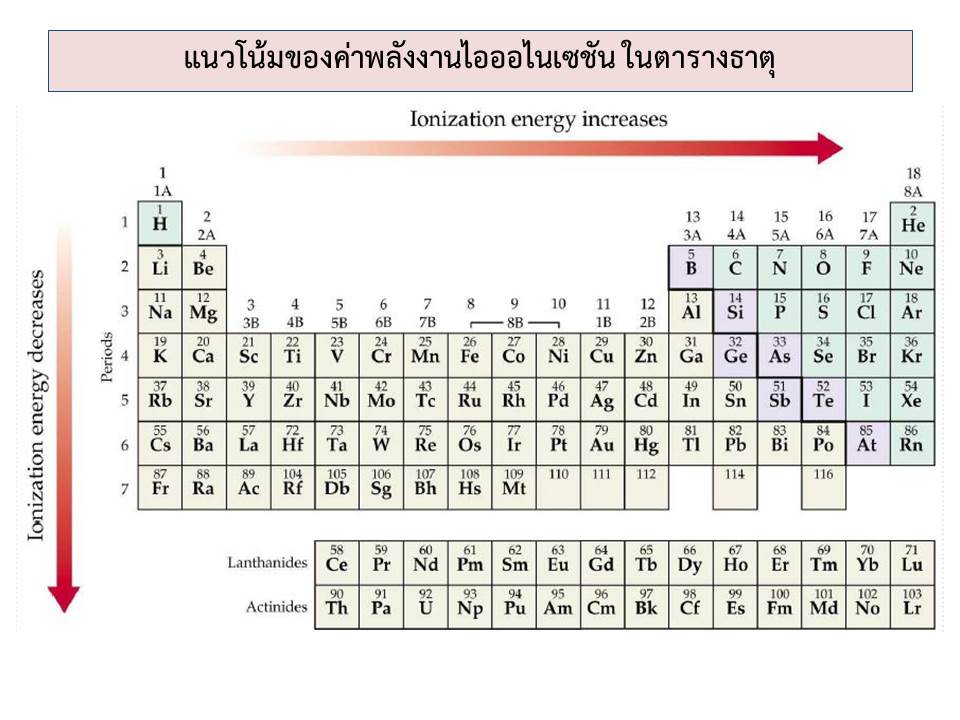
หลังจากที่ได้ทำความรู้จักกับตารางธาตุที่ใช้ในปัจจุบันกันแล้ว ในบทนี้จะขอกล่าวถึงสมบัติของธาตุตามตารางธาตุ ในเรื่องขนาดอะตอม ขนาดไอออน พลังงานไอออไนเซชัน ( IE ) ค่าอิเล็กตรอนอัฟฟินิตี ( EA ) และค่าอิเล็กโตรเนกาติวิตี้ ( EN ) ดังรายละเอียดที่จะกล่าวต่อไปนี้
การจัดเรียงธาตุลงในตารางธาตุ
เมื่อทราบการจัดเรียงอิเล็กตรอนของธาตุต่างๆ แล้ว จะเห็นว่าสามารถจัดกลุ่มธาตุได้ง่ายขึ้น โดยธาตุที่มีระดับพลังงานเท่ากัน ก็จะถูกจัดอยู่ในคาบเดียวกัน ส่วนธาตุที่มีจำนวนอิเล็กตรอนในระดับพลังงานนอกสุดเท่ากัน ก็จะถูกจัดอยู่ในหมู่เดียวกัน ดังภาพ
ประเภทของธาตุในตารางธาตุ
ธาตุโลหะ (metal) โลหะทรานซิชันเป็นต้นฉบับของโลหะ ธาตุโลหะเป็นธาตุที่มีสถานะเป็นของแข็ง ( ยกเว้นปรอท ที่เป็นของเหลว) มีผิวที่มันวาว นำความร้อน และไฟฟ้าได้ดี มีจุดเดือดและจุดหลอมเหลวสูง ( ช่วงอุณหภูมิระหว่างจุดหลอมเหลวกับจุดเดือดจะต่างกันมาก) ได้แก่ โซเดียม (Na) เหล็ก (Fe) แคลเซียม (Ca) ปรอท (Hg) อะลูมิเนียม (Al) แมกนีเซียม (Mg) สังกะสี (Zn) ดีบุก (Sn) เป็นต้น
ธาตุอโลหะ ( Non metal ) มีได้ทั้งสามสถานะ สมบัติส่วนใหญ่จะตรงข้ามกับอโลหะ เช่น ผิวไม่มันวาว ไม่นำไฟฟ้า ไม่นำความร้อน จุดเดือดและจุดหลอมเหลวต่ำ เป็นต้น ได้แก่ คาร์บอน( C ) ฟอสฟอรัส (P) กำมะถัน (S) โบรมีน (Br) ออกซิเจน (O 2) คลอรีน (Cl 2) ฟลูออรีน (F 2) เป็นต้น
ธาตุกึ่งโลหะ (metalloid) เป็นธาตุกึ่งตัวนำ คือ มันจะสามารถนำไฟฟ้าได้เฉพาะในภาวะหนึ่งเท่านั้น ธาตุกึ่งโลหะเหล่านี้จะอยู่บริเวณเส้นขั้นบันได ได้แก่ โบรอน (B) ซิลิคอน ( Si) เป็นต้น
ธาตุกัมมันตรังสี เป็นธาตุที่มีส่วนประกอบของ นิวตรอน กับโปรตอน ไม่เหมาะสม (>1.5) ธาตุที่ 83ขึ้นไปเป็นธาตุกัมมันตภาพรังสีทุกไอโซโทปมีครึ่งชีวิต
สมบัติของธาตุในแต่ละหมู่
ธาตุหมู่ I A หรือโลหะอัลคาไล (alkaline metal)
– โลหะอัลคาไล ได้แก่ ลิเทียม โซเดียม โพแทสเซียม รูบิเดียม ซีเซียม และแฟรนเซียม
– เป็นโลหะอ่อน ใช้มีดตัดได้
– เป็นหมู่โลหะมีความว่องไวต่อการเกิดปฏิกิริยามากที่สุด สามารถทำปฏิกิริยากับออกซิเจนในอากาศ จึงต้องเก็บไว้ในน้ำมัน
-ออกไซด์และไฮดรอกไซด์ของโลหะอัลคาไลละลายน้ำได้สารละลายเบสแก่
– เมื่อเป็นไอออน จะมีประจุบวก
– มีจุดเดือดและจุดหลอมเหลวต่ำ มีความหนาแน่นต่ำเมื่อเทียบกับโลหะอื่นๆ
– มีเวเลนซ์อิเล็กตรอน = 1
ธาตุหมู่ II A หรือโลหะอัลคาไลน์เอิร์ธ (alkaline earth)
– โลหะอัลคาไลน์เอิร์ธ ได้แก่ เบริลเลียม แมกนีเซียม แคลเซียม สตรอนเชียม แบเรียม เรเดียม
– มีความว่องไวต่อการเกิดปฏิกิริยามาก แต่น้อยกว่าโลหะอัลคาไล
– ทำปฏิกิริยากับน้ำได้สารละลายเบส สารประกอบโลหะอัลคาไลน์เอิร์ธพบมากในธรรมชาติ
– โลหะอัลคาไลน์เอิร์ธมีความว่องไวแต่ยังน้อยกว่าโลหะอัลคาไล
– โลหะอัลคาไลน์เอิร์ธมีเวเลนซ์อิเล็กตรอน = 2
ธาตุหมู่ III
– ธาตุหมู่ III ได้แก่ B Al Ga In Tl
– มีเวเลนซ์อิเล็กตรอน = 3
ธาตุหมู่ IV
– ธาตุหมู่ IV ได้แก่ C Si Ge Sn Pb
– มีเวเลนซ์อิเล็กตรอน = 4
ธาตุหมู่ V
– ธาตุหมู่ V ได้แก่ N P As Sb Bi
– มีเวเลนซ์อิเล็กตรอน = 5
ธาตุหมู่ VI
– ธาตุหมู่ VI ได้แก่ O S Se Te Po
– มีเวเลนซ์อิเล็กตรอน = 6
ธาตุหมู่ VII หรือหมู่แฮโลเจน (Halogen group)
– หมู่ธาตุแฮโลเจน ได้แก่ ฟลูออรีน คลอรีน โบรมีน ไอโอดีน และแอสทาทีน
– เป็นหมู่อโลหะที่ว่องไวต่อการเกิดปฏิกิริยามากที่สุด (F ว่องไวต่อการเกิดปฏิกิริยามากที่สุด)
– เป็นธาตุที่มีพิษทุกธาตุและมีกลิ่นแรง
– โมเลกุลของธาตุแฮโลเจนประกอบด้วย 2 อะตอม (Cl 2 Br 2 I 2)
– แฮโลเจนไอออนมีประจุบลบหนึ่ง (F – C – Br – I – At -)
ธาตุหมู่ VIII หรือก๊าซเฉื่อย หรือก๊าซมีตระกูล (Inert gas )
– ก๊าซมีตระกูล ได้แก่ ฮีเลียม นีออน อาร์กอน คริปทอน ซีนอน และเรดอน
– มีเวเลนซ์อิเล็กตรอนเต็ม 8 อิเล็กตรอน จึงทำให้เป็นก๊าซที่ไม่ว่องไวต่อการเกิดปฏิกิริยา
– ก๊าซมีตระกูลอยู่เป็นอะตอมเดี่ยว แต่ยกเว้น Kr กับ Xe ที่สามารถสร้างพันธะได้
ขนาดอะตอมของธาตุ
หน่วยพิโกเมตร

ขนาดอะตอมของธาตุต่างๆ
ขนาดของอะตอมนั้นถ้าจะพิจารณาถึงปัจจัยต่างๆ ที่ส่งผลกระทบต่อขนาดของอะตอมนั้น อาจแบ่งแยกออกได้เป็นข้อ เรียงตามลำดับความสำคัญได้ดังนี้
1. จำนวนระดับพลังงาน
2. จำนวนโปรตอน
3. จำนวนอิเล็กตรอน
ธาตุในหมู่เดียวกันมีสมบัติคล้ายกัน ธาตุที่อยู่ต่างหมู่กันมีสมบัติแตกต่างกัน ได้แก่
1. สถานะของธาตุ
ธาตุในตารางธาตุมีทั้งสถานะของแข็ง ของเหลว และแก๊ส เช่น ธาตุในหมู่ VIIIA มีสถานะเป็นแก๊สทุกธาตุ เรียกว่า แก๊สเฉื่อย หรือ แก๊สมีตระกูล ได้แก่ He, Ne, Ar, Kr, Xe และ Rn เป็นธาตุที่เสถียร ในสภาวะปกติจะไม่เกิดปฏิกิริยากับธาตุชนิดอื่น (แต่ปัจจุบันสามารถเตรียมสารประกอบของธาตุ Kr กับ Xe ได้) ธาตุที่มีสถานะเป็นของเหลว ได้แก่ Hg และ Br ธาตุโลหะส่วนใหญ่มีสถานะเป็นของแข็ง
2. ความเป็นโลหะและอโลหะของธาตุ
ธาตุที่เป็นโลหะอยู่ทางซ้าย และธาตุที่เป็นอโลหะอยู่ทางขวาของตารางธาตุ สมบัติความเป็นโลหะของธาตุลดลงจากซ้ายไปขวา ธาตุที่มีความเป็นโลหะมากที่สุด ได้แก่ ธาตุหมู่ IA ธาตุที่มีความเป็นอโลหะมากที่สุดได้แก่ ธาตุหมู่ VIIIA แต่ธาตุหมู่ VIIA เป็นอโลหะที่ว่องไวในการทำปฏิกิริยามากที่สุด ธาตุหมู่เดียวกันจะมีความเป็นโลหะเพิ่มขึ้นจากบนลงล่าง
ธาตุที่มีสมบัติบางประการคล้ายโลหะ และสมบัติบางประการคล้ายอโลหะ จัดเป็นธาตุกึ่งโลหะ ได้แก่ ธาตุที่อยู่ติดกับเส้นซิกแซ็กของตารางธาตุ
3. ความว่องไวของการเกิดปฏิกิริยา
ธาตุหมู่ IA ชื่อ โลหะแอลคาไลน์ มีความว่องไวในการเกิดปฏิกิริยามากกว่าหมู่ IIA ที่เรียกว่า โลหะแอลคาไลน์เอิร์ท ส่วนธาตุหมู่ VIIA ชื่อแฮโลเจน เป็นอโลหะที่มีความว่องไวในการเกิดปฏิกิริยามากที่สุด
4. ความสัมพันธ์ระหว่างเวเลนซ์อิเล็กตรอนกับสมบัติของธาตุในตารางธาตุ
อะตอมของธาตุที่เป็นกลางทางไฟฟ้า จะมีจำนวนอิเล็กตรอนเท่ากับเลขอะตอม