การจัดธาตุในตารางธาตุ
ในตารางธาตุมาตรฐาน ธาตุแต่ละตัวถูกจัดเรียงจากซ้ายไปขวาและจากบนลงล่างตามเลขอะตอม (Atomic Number) หรือจำนวนโปรตอนในนิวเคลียสของธาตุ โดยตารางธาตุในปัจจุบันแบ่งธาตุทั้งหมดออกเป็น 18 หมู่ (Group) ตามแนวดิ่ง โดยธาตุที่มีสมบัติคล้ายกันจะถูกจัดจำแนกให้อยู่ในหมู่เดียวกัน จากการจัดเรียงเวเลนซ์อิเล็กตรอน (Valence Electron) หรือมีจำนวนอิเล็กตรอนในวงนอกสุดเท่ากัน ทั้ง 18 หมู่ในตารางธาตุมีสัญลักษณ์เป็นตัวเลขโรมันหรือเลขอารบิก จาก 1 ถึง 18 และตัวอักษร เช่น IA หรือ 1A
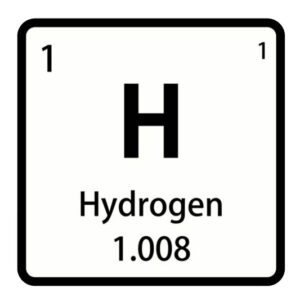
ชื่อและสัญลักษณ์ของธาตุในตารางธาตุ
- ตัวเลขบนมุมซ้ายด้านบน คือ จำนวนโปรตอนภายในอะตอมของธาตุหรือเลขอะตอม (Atomic Number)
- สัญลักษณ์ตัวอักษรตรงกลาง คือ อักษรย่อของชื่อธาตุ (Abbreviation) ในหลายกรณีสัญลักษณ์ที่มีชื่อภาษาอังกฤษอย่างเช่น ฮีเลียม (Helium) จะใช้ “He” เป็นตัวแทนสัญลักษณ์ของธาตุ
- ตัวเลขด้านล่าง คือ มวลอะตอม (Atomic Mass) หรือจำนวนโปรตอนและนิวตรอนภายในนิวเคลียสของธาตุนั้นๆ
ในระยะต่อมา IUPAC ได้ยอมรับการเรียกชื่อและสัญลักษณ์ของธาตุตามชื่อของนักวิทยาศาสตร์ที่มีชื่อเสียง ซึ่งผล
การลงมติเมื่อปลายปี พ.ศ. 2537 ได้ก าหนดชื่อธาตุจนถึงธาตุที่ 109 ดังนี้
ธาตุที่ ชื่อธาตุ สัญลักษณ์
ธาตุ 101 Mendelevium Md
ธาตุ 102 Nobelium No
ธาตุ 103 Lawrencium Lr
ธาตุ 104 Dubnium Db
ธาตุ 105 Joliotium Jl
ธาตุ 106 Rutherfordium Rf
ธาตุ 107 Bohrium Bh
ธาตุ 108 Hahnium Hn
ธาตุ 109 Meitnerium Mt
การเรียกชื่อธาตุตามระบบ IUPAC (International Union of Pure and Applied Chemistry)
การเรียกชื่อธาตุที่มีเลขอะตอมตั้งแต่ 100 ขึ้นไปตามระบบตัวเลขเป็นภาษาละตินและลงท้ายเสียงของชื่อ
ธาตุ –ium การเขียนสัญลักษณ์ของธาตุให้ใช้ตัวอักษรตัวแรกของจ านวนนับแต่ละตัวมาเขียนเรียงกัน โดยจ านวนนับ
ในภาษาละตินเป็นดังนี้
0 1 2 3 4 5 6 7 8 9
Nil un bi tri quad pent hex Sept oct enn
นิล อูน ไบ ไตร ควอด เพนต์ เฮกซ์ เซปต์ ออกต์ เอนน์
ชื่อเฉพาะของธาตุบางหมู่
มีธาตุอยู่ 5 หมู่ที่มีชื่อเรียกเฉพาะ ซึ่งชื่อเหล่านี้นักเคมีค้นเคยและเรียกมาเป็นเวลาช้านานแล้ว ดังนี้
หมู่ธาตุ ชื่อเฉพาะประจ าหมู่ธาตุ
IA
IIA
VIIA
VIIIA
IB
ธาตุแอลคาไล (alkali metals) ยกเว้น ธาตุไฮโดรเจน
ธาตุแอลคาไลน์เอร์ท (alkaline earth metals)
ธาตุแฮโลเจน (halogen)
แก๊สเฉื่อย (noble gas)
ธาตุเงินตรา (coinage metals)
ตารางที่ 3 แสดงชื่อเฉพาะของธาตุบางหมู่
สถานะของธาตุในแต่หมู่สถานะของธาตุในแต่ละหมู่ของธาตุเรพรีเซนเททีฟ ยกเว้น ไฮโดรเจน
หมู่ IA, IIA, IIIA และ IVA มีสถานะเดียว คือ ของแข็ง
หมู่ VA และ VIA มี 2 สถานะ คือ ของแข็งและแก๊ส
หมู่ VIIA มี 3 สถานะ คือ ของแข็ง ของเหลว และแก๊ส
หมู่ VIIIA มีสถานะเดียว คือ แก๊ส
ธาตุที่ค่อนไปทางขวาของตารางธาตุจะมีเส้นหนักเป็นขั้นบันได ธาตุทางขวาของเส้นจะเป็นอโลหะ ส่วน
ทางซ้ายของเส้นจะเป็นโลหะ ส าหรับธาตุที่อยู่ชิดเส้นแบ่งนี้จะมีสมบัติเป็นทั้งโลหะและอโลหะ ได้แก่ โบรอน (B),
ซิลิกอน (Si), เจอร์เมเนียม (Ge), สารหนู (As), พลวง (Pb), เทลลูเรียม (Te) และแอสทาทีน (At) เรียกธาตุ
พวกนี้ว่า ธาตุกึ่งโลหะ (metalloids)
7 ตารางธาตุ (Periodic table of Element) :
ตารางธาตุในปัจจุบันจะเรียงตามเลขอะตอมจากน้อยไปมาก และอาศัยการจัดเรียงอิเล็กตรอนเป็นหลักใน
การบอกต าแหน่งของธาตุต่างๆ โดยเลขที่คาบของธาตุดูจากจ านวนระดับพลังงานของอิเล็กตรอน ส่วนเลขหมู่ดูจาก
จากจ านวนเวเลนซ์อิเล็กตรอนของอะตอมที่เป็นกลางทางไฟฟ้า (จ านวนอิเล็กตรอนเท่ากับจ านวนโปรตอน) ดังนั้น
เมื่อทราบเลขอะตอมของธาตุควรบอกได้ว่าธาตุนั้นอยู่ในหมู่ใด คาบใด หรือถ้าทราบว่าธาตุหนึ่งอยู่ในหมู่หรือคาบ
หนึ่งๆ ควรระบุต าแหน่งของธาตุนั้นในตารางธาตุได้และบอกการจัดเรียงอิเล็กตรอนได้
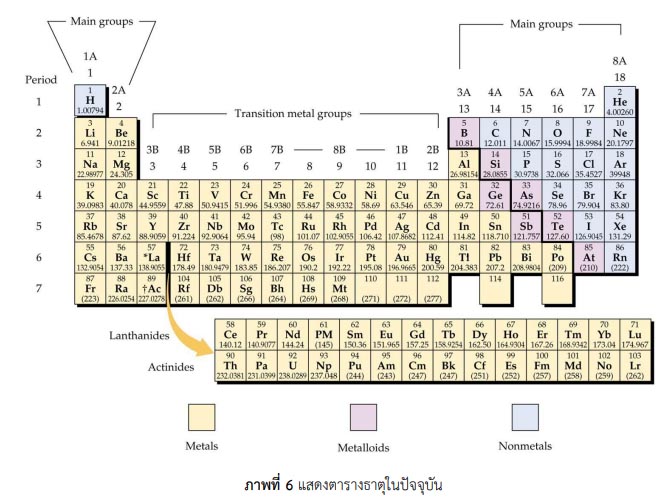
จากภาพที่ 6 สรุปได้ว่า
1) การจัดเรียงธาตุตามแนวนอน เรียกว่า คาบ (period)
– การจัดเรียงล าดับของธาตุจะอาศัยเลขอะตอมเป็นเกณฑ์ โดยเรียงเลขอะตอมจากน้อยไปมาก
– ธาตุที่เรียงไปตามแถวแนวนอน เรียกว่า “คาบ (period)” โดยเรียงจากบนลงล่าง คาบที่ 1 อยู่บนสุด
แล้วถัดลงไปจะเป็นคาบที่ 2, 3, 4, … จนถึงคาบสุดท้ายอยู่ล่างสุด จะเป็นคาบที่ 7
– ธาตุในแต่ละคาบจะมีจ านวนไม่เท่ากัน ดังนี้
คาบที่ 1 มี 2 ธาตุ คือ H และ He คาบที่ 2 มี 8 ธาตุ คือ Li ถึง He
คาบที่ 3 มี 8 ธาตุ คือ Na ถึง Ar คาบที่ 4 มี 18 ธาตุ คือ K ถึง Kr
คาบที่ 5 มี 18 ธาตุ คือ Rb ถึง Xe
คาบที่ 6 มี 32 ธาตุ โดยธาตุกลุ่มแรกมี 8 ธาตุ คือ ธาตุที่มีเลขอะตอม 55 – 86 (Cs ถึง Rn) โดย
คาบที่ 6 จะมีธาตุที่มีเลขอะตอม 58 – 71 (Ce ถึง Lu) จ านวน 14 ธาตุรวมด้วยกัน เรียกธาตุพวกนี้ว่า
กลุ่มแลนทาไนด์ (lanthanide series หรือ rare-earth element) เพราะว่าอยู่ถัดจากธาตุแลนทานัม (La)